ERINEVA α-AMINORÜHMA KONFIGURATSIOONIGA LÜSIINI SISALDAVATE INHIBIITORITE SÜNTEES JA NENDE TOIME UURIMINE PROTEIINKINAASILE A
ERINEVA α-AMINORÜHMA KONFIGURATSIOONIGA LÜSIINI SISALDAVATE INHIBIITORITE SÜNTEES JA NENDE TOIME UURIMINE PROTEIINKINAASILE A
Arenev meditsiin ja aina kasvav uudishimu inimkeha ehituse ja talitluse vastu on viinud teadlased proteiinkinaaside (edaspidi PK) avastamiseni. Need ensüümid on ühed tähtsaimatest biokeemiliste reaktsioonide reguleerijatest, sest valke aktiveerides, moduleerides või inhibeerides võimaldavad just nemad täita proteiinidel oma funktsiooni. Nii on PK-de toimel võimalikud sellised rakuprotsessid nagu apoptoos, raku jagunemine, ainete lagundamine jpm ehk tänu neile ensüümidele on tagatud raku normaalne elutegevus. Paraku on igas süsteemis võimalikud vead, seda ka meis endis. Üsna sage on olukord, kus teatud ensüüm on muteerunud ja seega kaotanud funktsioneerimisvõime või täidab oma ülesannet vääralt. Selliste molekulide kõrge aktiivsuse tõttu on häiritud raku talitlus, süsteem ei ole kontrollitav ja tekivad väga tõsised haigused, sh erinevad pahaloomulised kasvajad, sisenõrenäärmete töö häired, immuunsüsteemi nõrgenemine.
Bioorgaaniliste ainete väärtalitlus ja eelkõige sellega kaasnevad haigused on leidnud väljundi tänapäeva meditsiinis, kus spetsialiseerutakse aina rohkem bioaktiivsete ainete, näiteks mitmesuguste inhibiitorite, ensüümi aktiivsust pärssivate ainete arendamisele. Püütakse leida inhibiitorid, mis võivad olla tundlikud muteerunud PK-de suhtes, need n-ö tuvastada ja inaktiveerida, hoides niiviisi ära haiguste sümptomite avaldumise. Selliseid bioaktiivseid aineid on võimalik kasutada ravimitena. Maailmaturul on juba laialdaselt kasutatud erinevaid PK-de inhibiitoreid, kuid kindlasti pole leitud lahendusi kõikidele meditsiinilistele muredele. Nii pakub teaduse kirjeldatud suunitlus palju arenguvõimalusi.
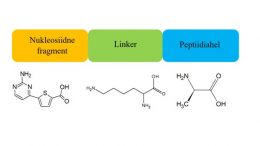
Uurimistöös keskendutakse võimalikult selektiivsete ja efektiivsete proteiinkinaas A (edaspidi PKA) inhibiitorite sünteesile. Töö eesmärk on valmistada kaks erineva lüsiini konfiguratsiooniga inhibiitorit ja võrrelda nende toimet PKA-le. Huvipakkuv on teema seetõttu, et esimest korda viiakse töös käsitletud inhibiitortüübi keskmisesse osasse sisse aminorühm. Esimene uurimisküsimus on: kuidas mõjutab inhibiitori keskmises osas olev aminorühm selle PK-ga seostumist? Uurimistöös püstitatakse hüpotees, et linkeris paiknev aminorühm muudab inhibiitori sidumisomadusi, kuna võib mõjuda PK-le tõmbavalt või tõrjuvalt. Teine uuritav aspekt puudutab lüsiinivaba aminorühma konfiguratsiooni mõju inhibiitori seostumisefektiivsusele. Sellega seoses püstitati teine uurimisküsimus: kuidas mõjutab aminorühma erinev konfiguratsioon inhibiitori seostumist PK-ga? Viimasele probleemile püstitatakse hüpotees, et L-lüsiini sisaldav aine on efektiivsem, sest looduses esinevad valdavalt L-aminohapped.
Uurimistöö praktiline osa tehakse Tartu Ülikooli keemia instituudi bioorgaanilise keemia laboratooriumis. Töö eksperimentaalse osa esimeseks meetodiks valiti juba peptiidide sünteesis tavaliseks kujunenud Fmoc-tahkefaassüntees, mida kohandati vastavalt TÜ laboratooriumi võimalustele. Sünteesi etappide vahel kontrolliti reaktsioonide kulgemist kvalitatiivselt Kaiseri testiga. Sünteesitud ühendite sisaldumine lõppsaaduste segus määrati kromatograafia ja massispektromeetria ühissüsteemiga, kus oli rakendatud ka ultraviolettkiirguse ja nähtava valguse neelduvuse detektorid. Saadused puhastati kõrgefektiivse vedelikkromatograafiaga ning puhaste inhibiitorite seostumist PKA-ga uuriti biokeemilistes katsetes, mis seisnesid ensüümilt fluorestsentsmärgisega aine inhibiitoritepoolses väljatõrjumises. Katsete tulemuste analüüsimiseks kasutati fluorestsentsanisotroopia mõõtmisi.
Uurimistöö jaguneb neljaks peatükiks. Esimesena antakse ülevaade PK-de toimimisest organismis, sh fosforüülimisest, nende inhibiitoritest ning stereokeemiast, avades spetsiifilisi teemasid, nagu PKA-d, PKA-de inhibiitorid ning diastereomeersed kiraalsed ühendid. Esimeses peatükis toetuti eelkõige Darja Lavõgina (2010) doktoritööle „Development of protein kinase inhibitors based on adenosine analogue-oligoarginine conjugates“. Teises peatükis tutvustatakse töös kasutatud meetodeid: Fmoc-tahkefaassüntees, pööratud faasi kõrgefektiivne vedelikkromatograafia, massispektromeetria ning fluorestsentsanisotroopia. Nende iseloomustamiseks toetuti esmajoones Wilsoni ja Walkeri (2010) välja antud teosele „Principles and techniques of biochemistry and molecular biology“. Kolmandas peatükis kirjeldatakse uurimistöö praktilist osa ning neljandas esitatakse tulemused, analüüsides iga eksperimendi väljundit ja arenguvaldkondi.

